|

|
|
|
4.2 Kryokonservierung von
Spermien und Embryonen
|
|
|
|
Das Prinzip der Kryokonservierung beruht auf den Auswirkungen von niedrigen Temperaturen auf Zellen. Bei Temperaturen unterhalb von -80°C kommen die Stoffwechselvorgänge zum Stillstand. Daraus resultiert eine Situation, in der die physikalisch-chemischen Eigenschaften unverändert erhalten bleiben. Die tiefen Temperaturen bringen aber auch Nachteile. Grundsätzlich sind bei Temperaturerniedrigung Veränderungen und/oder Schäden insbesondere an der Zellmembran zu erwarten. Jene Schäden, die während des Abkühlens auftreten, werden Kühlschäden genannt. Beim Prozess des Einfrierens kommt es, abhängig von der Temperaturkinetik, zur raumfordernden Bildung von Eiskristallen, zu einer Dehydrierung der Zellen und zu einer Konzentrationserhöhung von gelösten Stoffen. Diese 3 Phänomene werden unter dem Begriff Gefrierschäden zusammengefasst. Sie können dem biologischen Gewebe erheblichen Schaden zufügen und die Wiederherstellung der physiologischen Vorgänge nach dem Auftauen in Frage stellen. Deshalb werden für jede Tiefgefrierung Kryoprotektiva (Gefrierschutzmittel) benötigt, die die Zelle vor entsprechenden Schäden schützen.
|
|
|
|
Beim Abkühlen unter den Gefrierpunkt lagern sich Wassermoleküle geordnet aneinander, es bilden sich Kristalle. Dabei formieren sich in Abhängigkeit von Druck und Lösungskonzentration die Wassermoleküle zu mikroskopisch kleinen Eiskernen (Nukleation), an die sich weitere Wassermoleküle anlagern und somit immer größere Eiskristalle bilden (Eiskristallwachstum). Zuerst kristallisiert das wässrige Medium im Interzellulärraum. Wasser dehnt sich beim Gefrieren um bis zu 10 % aus, weil die Molekülbindungen der Tetraederstruktur mehr Raum als im flüssigen Wasser benötigen.
|
|
|
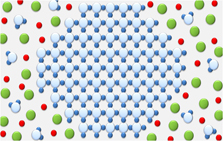
| Abb. 3 - Flüssiges Wasser |
|
Abb. 4 - Eiskristall |
|
Legende |

|
|
|
|
Abb. 3
Im Wasser sind die Moleküle regellos verteilt.
Abb. 4
Beim gewöhnlichem Einfrieren ordnen sich die Wassermoleküle zu Kristallen an.
|
|
Die Zellmembranen verhindern die Ausdehnung des Kristallwachstums vom Interstitium ins Zellinnere, der Zellinhalt bleibt vorerst auch unterhalb des Gefrierpunktes flüssig, wird aber unterkühlt (Supercooling). Die im flüssigen Wasser gelösten Ionen senken den Gefrierpunkt der Lösung und verhindern einen Zusammenschluss der Wassermoleküle zu Eiskristallen.
Da die zwischen den Zellen entstandenen Kristalle aus reinem Wasser bestehen, steigt die Osmolarität der noch nicht gefrorenen interzellulären Flüssigkeit zwischen den Kristallen an. Somit bildet sich ein Konzentrationsgradient zwischen der interzellulären und der intrazellulären Flüssigkeit. Die weiteren Vorgänge sind weitgehend abhängig von der Abkühlrate. Über die Erhaltung der Vitalität der Zellen bei verschiedenen Abkühlraten entscheiden Zelleigenschaften, die vor allem die Geschwindigkeit des Wasseraustritts aus der Zelle beeinflussen. Dazu zählen die Permeabilität der Zellmembran, der zur Permeabilität gehörende Temperaturkoeffizient und das Verhältnis von Zellvolumen zu Zelloberfläche.
Ist die Kühlrate niedrig (langsames Einfrieren), geben die Zellen die intrazelluläre Flüssigkeit entlang des osmotischen Gradienten in den Interzellulärraum ab. Die Zelle schrumpft und die intrazellulären osmotischen Werte steigen an (Zelldehydrierung). Die damit verbundenen, sogenannten Lösungseffekte stellen den grössten Gefrierschaden dar. Die Lösungseffekte beinhalten zusammenhängende Prozesse wie die ansteigende Konzentration der intrazellulären Lösung, den abfallenden intrazellulären Wassergehalt sowie die Präzipitation von gelösten Stoffen beim Überschreiten von Löslichkeiten. Es wird vermutet, dass die Proteine der Zellmembran dadurch denaturiert und die Konformation der Polymere verändert wird. Ausserdem werden durch die extrazellulär wachsenden Eiskristalle die Zellmembranen mechanisch beschädigt, was den Verlust der Kompartimentierung zur Folge haben kann.
Wird die Zelle so schnell abgekühlt, dass für das osmotische Ausströmen von intrazellulärer Flüssigkeit keine Zeit bleibt, bilden sich intrazellulär ebenfalls Eiskristalle. Das osmotische Gleichgewicht bleibt nun zwar erhalten, aber durch das Kristallwachstum im Zellinnern können die Zellorganellen und die Zellmembran erheblich geschädigt werden. Da also sowohl die Zelldehydrierung wie auch die intrazelluläre Kristallbildung zu Schäden an der Zelle und somit zu einem Vitalitätsverlust führen, ist eine optimale Kühlungsrate entscheidend für die maximale Überlebensfähigkeit der Zellen und somit für den Erfolg des Gefrierprozesses.
|
|
|
|
Werden Zellen oder Embryonen unter Vermeidung der Bildung von Eiskristallen eingefroren, spricht man von Vitrifikation (lat.: vitrum = Glas). Die in den Proben vorhandene intra- und extrazelluläre Flüssigkeit wird zunehmend viskös, stabil, amorph und geht schlussendlich in einen glasartigen (vitrifizierten) Zustand über. Die Wassermoleküle ordnen sich nicht zu einem Kristallgitter und damit bleibt auch die Volumenzunahme aus.
|
|
Abb. 5 - Vitrifikation |
|
Legende |
|

|
|
Abb. 5
Beim ultraschnellen Einfrieren fehlt die Zeit für die Kristallbildung, man spricht von Vitrifikation.
|
|
Alle Eigenschaften der flüssigen Phase werden in der soliden Phase beibehalten. Eine Kristallbildung findet nicht statt, weder intra- noch extrazellulär. Jegliche Verfahren, die das Erreichen des vitrifizierten Zustandes gewährleisten, gelten als Vitrifikation.
In der assistierten Reproduktion versucht man, dem vitrifizierten Zustand durch Zugabe hoher Mengen an Kryoprotektiva (siehe Kapitel Kryoprotektiva) und durch sehr schnelle Abkühlraten möglichst nahe zu kommen. Zugesetzte hochkonzentrierte, penetrierende Kryoprotektiva ersetzen einen hohen Teil des intrazellulären Wassers und binden an die restlichen Wassermoleküle. Um die Proben möglichst schnell abzukühlen, werden sie direkt in flüssigen Stickstoff gegeben. Aufgrund der schlechten Wärmeleitfähigkeit biologischen Gewebes limitiert die Grösse der Proben den Erfolg der Vitrifikation in der assistierten (Tier-) Reproduktion. Ausserdem können die hohen Konzentrationen an Kryoprotektiva ihrerseits toxisch auf die Zellen wirken.
Wird eine vitrifizierte Probe (z.B. ein Embryo) wieder erwärmt (umgangssprachlich aufgetaut), muss die Erwärmungsrate der Abkühlrate angepasst sein, da sonst zuvor unbeschadete vitrifizierte Zellen oder Embryonen durch die Bildung von Kristallen während der Erwärmung (Rekristallisation) geschädigt werden könnten.
|
|
|
|
|

